Considera que los ensayos clínicos han mostrado que la inyección ofrece una protección del 100% contra la Covid-19 en este grupo de edad
REDACCIÓN | EUROPA PRESS
La Agencia Euroapea del Medicamento (EMA, por sus siglas en inglés) ha otorgado la autorización condicional de comercialización a la vacuna de Pfizer BioNTech contra el COVID-19 para niños de 12 a 15 años, hasta ahora estaba autorizada a partir de más de 16 años.
El jefe de Estrategia de Vacunas y Amenazas Biológicas para la Salud, Marco Cavaleri, ha valorado los datos que avalan su aprobación. "Ya estaba para jóvenes a partir de los 16 años en adelante y ahora tenemos datos que muestran que la vacuna es segura también en las edades de 12 a 15 años y eso es lo que permite a la comunidad científica concluir hoy esta decisión".
No obstante, según ha explicado la decisión de usarla dependerá de cada uno de los países de la Unión Europea. "Los Estados Miembros tendrán que decidir si utilizarla y cuándo utilizarla la protección de una vacuna segura y eficaz para la población más joven; es un paso importante en la lucha contra el pesar", dice Cavaleri.
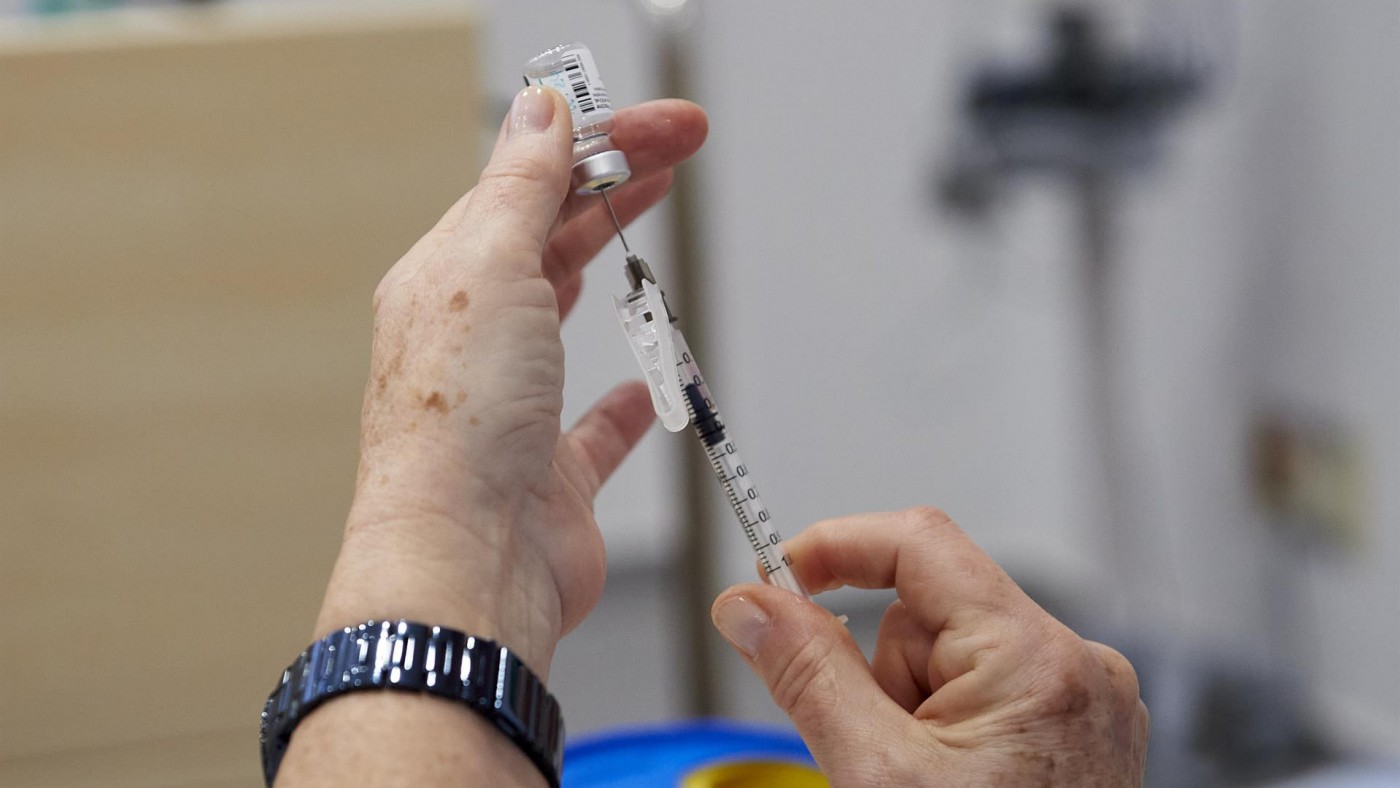
La vacuna seguirá las mismas pautas de administración que para los adultos, lo que significa que se requieren dos dosis y deben administrarse con un intervalo de al menos tres semanas. La decisión se determinó en base a un ensayo donde se han observado resultados similares o incluso mejores de lo que están viendo en los adultos jóvenes.
"Los datos realmente muestran que la vacuna es altamente protectora en esta población para prevenir la enfermedad desde una perspectiva de seguridad. Fue bien tolerada y el efecto deseado en este grupo de edad fue muy similar al que vemos en los adultos jóvenes", ha explicado. No obstante, ha recordado que la EMA monitorea continuamente la seguridad y efectividad de esta vacuna tanto en niños como en adultos.
Debido a que se espera que sea necesaria una mayor producción de este suero, Cavaleri ha señalado que la EMA esta trabajando para autorizar la ampliación de la capacidad de fabricación y también siempre que sea posible aumentar la flexibilidad en las condiciones de almacenamiento de la vacuna ya que esto es en beneficio de la campaña de vacunación en los modelos europeos.
Actualmente la EMA está evaluando actualmente casos muy raros de miocarditis (inflamación del músculo cardíaco) y pericarditis (inflamación de la membrana alrededor del corazón) que ocurrieron después de la vacunación con Comirnaty, principalmente en personas menores de 30 años. Actualmente no hay indicios de que estos casos se deban a la vacuna y la EMA está monitoreando de cerca este problema.
La comparecencia de Cavaleri ha servido también para que la Agencia Europea del Medicamento haya anunciado que los primeros datos recopilados sobre la persistencia de la inmunidad generada por las vacunas parecen descartar la necesidad de recibir una tercera dosis, aunque todavía serán necesarias más pruebas para establecer una posición definitiva.
"Hasta ahora hemos visto algunos datos preliminares y estamos esperando a más información que estará disponible a corto plazo y por ahora no parece que tengamos que apresurarnos en administrar una tercera dosis, aunque necesitamos más pruebas que seguiremos recopilando en las próximas semanas y meses para adoptar una postura definitiva a este respecto", ha dicho Cavaleri.
Respecto al uso de corticosteroides inhalados para tratar a enfermos de covid, la EMA ha señalado que no cuenta con estudios suficientes para determinar si son beneficiosos, por lo que desaconseja su uso hasta contar con pruebas concluyentes. Sobre el uso de otros antivirales, la EMA está analizando cuatro medicamentos que confía en autorizar en el tercer o cuarto trimestre de este año.